Richtlijn ALL
Auteur: Bart Biemond
Algemeen:
In het algemeen wordt de term ALL gebruikt als er sprake is van aanwezigheid van lymfoide blasten in perifeer bloed of beenmerg.Indien er bij presentatie alleen sprake is van lymfklierlokalisatie of lokalisatie in extranodale organen is de term lymfoblastair lymfoom meer op zijn plaats. Omdat de aard van de ziekte identiek is (evenals de prognose), zijn de onderstaande richtlijnen zowel voor ALL als voor lymfoblastair NHL van toepassing. Jaarlijks zijn er in Nederland 200 nieuwe gevallen van ALL. ALL komt voor op alle leeftijden, maar vooral bij jonge patiënten (Figuur 1).
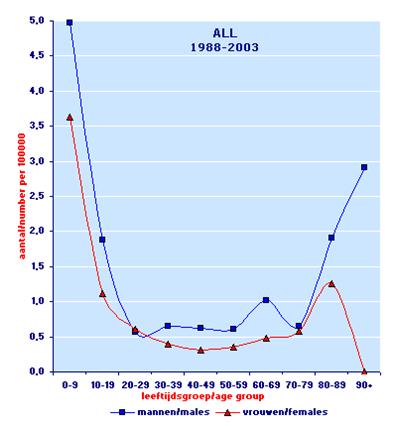
Figuur 1: Leeftijd specifieke incidentie van ALL in de Amsterdamse regio (IKA). Gegevens van de kankerregistratie (IKCNET).
Kliniek:
Bij presentatie worden de klachten vooral veroorzaakt door beenmergverdringing: anemie en/of trombopenie en/of neutropenie. Neurologische klachten zoals hoofdpijn en uitval van hersenzenuwen treden op in ongeveer 5 a 10% als gevolg van centraal zenuw (CZS) lokalisatie of myelum compressie. Bij ongeveer 50% van de patiënten is er sprake van perifere lymfadenopathie en organomegalie (hepatosplenomegalie). Een T-ALL presenteert zich vaak met een primair verbreed mediastinum. Testis lokalisatie komt bij volwassenen minder frequent voor. Naast algemene symptomen van vermoeidheid en malaiseklachten komen bij ALL ook regelmatig bot- en gewrichtspijnen voor. Hyperleukocytose (> 100x 10E9/l) komt vaker voor bij T-ALL maar leidt zelden tot symptomen van leukostase.
Diagnose:
Voor de diagnostiek bij een ALL is naast de analyse van perifeer bloed ook onderzoek van het beenmerg en liquor noodzakelijk. De diagnostiek bestaat uit: 1. morfologische analyse; 2. immunofenotypering; 3. cytogenetische analyse en 4. moleculaire diagnostiek.
Morfologie:
Lymfoïde blasten zijn over het algemeen kleiner dan myeloïde blasten met soms blauw cytoplasma en vacuolen. Het onderscheid met monoblasten kan moeilijk zijn. In lymfoïde blasten komen geen Auerse staven voor.
Perifeer bloed:
- anemie, trombopenie en leukopenie of leucocytose
- circulerende blasten
- gestoorde nierfunctie, verhoogd LDH en verhoogd urinezuur
Beenmergaspiraat:
- celrijk beenmerg met verdringing van de normale hematopoïese
- blasten infiltratie
Liquorpunctie:
- blasten infiltratie
Immunofenotypering:
Voor zowel de diagnose als bepaling van de minimal residual disease (MRD) is immunofenotypering noodzakelijk. Dit kan zowel op het perifere bloed, beenmerg als op blasten in de liquor worden verricht. In de onderstaande tabel is de ALL classificatie op grond van de fenotypering weergegeven.
| B-ALL TdT+ HLA-DR+ CD34+/- CD117- CD19+ CD22+/- |
T-ALL TdT+ CD34+/- CD117- CD2+ CD7+ cCD3+ |
| Pro-B-ALL (early stage) | Pro-T-ALL |
| TdT+ HLA-DR+ CD34+ CD19+ CD22+ CyCD79a+ |
TdT+ CD4- |
| Common B-ALL (intermediate stage) | Pre-T-ALL |
| TdT+ HLA-DR+ CD19+ CD22+ CyCD79a+ CD10+ |
TdT+ CD1a – CD34+/- CD4- CD2+ CD8- cCD3+ CD7+ |
| Pre-B-ALL (mature stage) | Cortical T- ALL |
| TdT + HLA-DR+ CD19+ CD22+ CyCd79a+ CD10+ Cyµ (zwak)+ |
TdT+ CD34- CD1a+ CD2+ cCD3+ CD7+ CD4+ CD8+ |
| Medullary T-ALL | |
| TdT+ CD34- CD2+ CD1a- CD7+ cCD3+ surface CD3+ CD4 of CD8+ |
Cytogenetica:
Cytogenetische analyse is de belangrijkste prognostische factor voor ALL en is een essentieel onderdeel van de diagnostiek.
Op grond van cytogenetica kan ook het relapse risico van de ALL worden gedefinieerd.
Enkele cytogenetische afwijkingen die met een slechte prognose geassocieerd zijn:
- t(9;22)(q34;q11.2)
- t(v;11q23)
- t(12;21)(p13;q22)
- hyperdiploidy; hypodiploidy
- t(5;14)(q31;q32)
- t(1;19)(q23;p13.3)
- t(4;11)
Moleculaire diagnostiek:
Moleculaire diagnostiek kan worden gebruikt om met behulp van PCR de mate van MRD te bepalen bij bekende cytogenetische afwijkingen zoals t(9;22), t(4;11), t(8;14), t(1;19), of (in studieverband) m.b.v patient specifieke primers
WHO classificatie:
De oude classificatie (L1 tot met L3) op basis van morfologie wordt niet meer gebruikt. Voor de huidige WHO classifcatie worden de resultaten van immunofenotypering en de cytogenetica gebruikt.
De WHO-indeling is gebaseerd op de immunologische indeling met B-en T-cel lineage:
1. B-lymphoblastic leukaemia/lymphoma not otherwise specified.
2. B-lymphoblastic leukaemia/lymphoma with recurrent genetic abnormalities.
- B lymphoblastic leukaemia /lymphoma with t(9;22)(q34;q11.2); BCR/ABL1.
- B lymphoblastic leukaemia /lymphoma with t(v;11q23); MLL rearranged.
- B lymphoblastic leukaemia /lymphoma with t(12;21)(p13;q22); TEL-AML1.
- B lymphoblastic leukaemia /lymphoma with hyperdiploidy.
- B lymphoblastic leukaemia /lymphoma with hypodiploidy.
- B lymphoblastic leukaemia /lymphoma with t(5;14)(q31;q32); IL3-IGH.
- B lymphoblastic leukaemia /lymphoma with t(1;19)(q23;p13.3); E2A-PBX1.
3. T-lymphoblastic leukaemia/lymphoma.
Prognose:
De prognose van patiënten met ALL hangt af van een aantal klinische, laboratorium en cytogenetische factoren af. De rol van de cytogenetische factoren is weergegeven in Figuur 2. De volgende klinische factoren zijn geassocieerd met een ongunstige prognose:
- Leeftijd ouder dan 35 jaar
- Leukocytose bij presentatie: >30x10E9/l voor B-ALL en >100x10E9/l voor T-ALL
- Interval tot bereiken van een complete remissie (>4 weken)
- Recidief ALL
- CZS lokalisatie
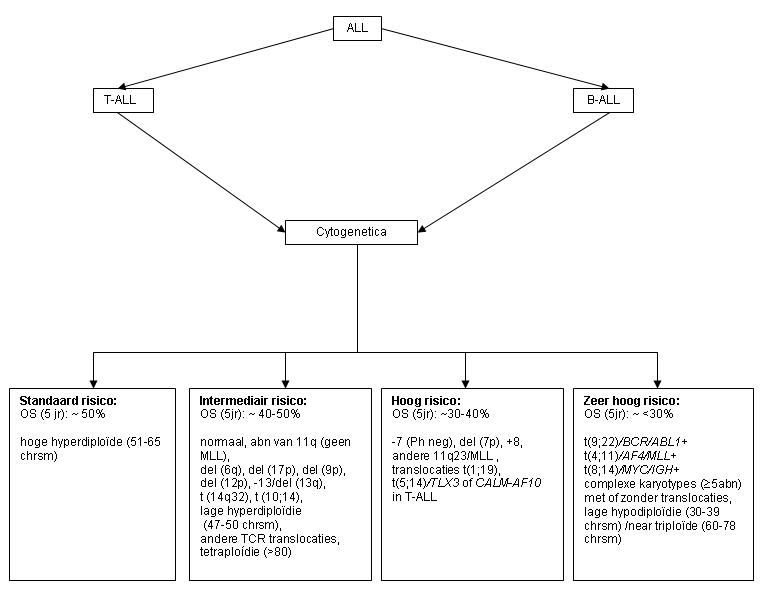
Figuur 2: Prognose en cytogenetica (Pullarkat et al.)
Behandeling:
Algemeen:
- Er wordt geen standaard hydratie gegeven in het wijzerprotocol. Daarom voorschrijven:
- hydratie: 2,5 l NaCl 0.9% / 24 hr. Allopurinol 1 dd 300 mg.
- bij hoge tumorload: rasburicase (Fasturtec®) 2,5 L NaCl 0.9% / 24 hr. Niet alkaniseren. (zie sop tumorlysis)
- Cave tumorlysis.
- Leukaferese bij klinische verdenking leukostase (zeldzaam)
- Voorkomen van menstruatie: orgametril.
- Eventueel semen preservatie.
- Infectieprofylaxe: naast de standaard profylaxe (Gram positief, Gram negatief, schimmel), ook valaciclovir en cotrimoxazol ten tijde van prednisongebruik. (zie sop infectieprofylaxe )
- NB Cotrimoxazol stoppen 3 dagen voor toediening hoge dosis MTX tot 5 dagen erna
Chemotherapie:
Patiënten worden zo veel mogelijk behandeld in studieverband volgens HOVON 100 (standaard behandeling met of zonder clofarabine).
Patiënten met een t(9:22) krijgen tevens een tyrosine kinase remmer (imatinib 1 dd 600 mg).
Algemene opmerkingen:
- Asparaginase:
Hierdoor wordt het asparagine in de cel verlaagd met een gunstig effect op de ALL blasten. Asparaginase veroorzaakt echter ook een verminderde aanmaak van diverse (anti)stollingsfactoren. Hierdoor is het risico op veneuze trombose verhoogd met als meest opvallende sinus cavernosus trombosis ( frequentie 5% van de patiënten) maar ook longembolieën en diep veneuze trombose kunnen voorkomen (incidentie 15%). Niet alleen asparginase maar ook prednison blijkt een risicofactor voor trombose bij ALL behandling. Daarnaast kunnen er bloedingscomplicaties optreden als gevolg van fibrinogeen depletie. Het risico op trombo-embolitische complicaties is het hoogst ten tijde van de inductie behandeling waarbij steroïden en asparaginase gebruik een extra risico vormen. Onduidelijk is nog wat de rol van liquorpuncties is op dit risico. In het HOVON 100 protocol is nu een nieuw profylactisch beleid opgenomen. Hierbij krijgen alle patienten gedurende de inductie hoge dosis LMWH profylaxe (5700 E 1dd s.c.) gedurende 35 dagen, en start al bij de prefase. Dit geldt voor zowel de jongere (<=40 jaar) als oudere patienten (>40 jaar).
Hierbij hoeven het fibrinogeen en AT niet meer gecontroleerd te worden.
Bij asparginase toedienen in latere fase van de behandeling is geen profylaxe noodzakelijk. FFP suppletie is niet meer nodig in het huidige protocol. Van belang is het trombocyten aantal > 20 x 10E9/l te houden gedurende de LMWH toediening en rekening te houden met liquor puncties (24 hr van te voren staken van profylaxe)
Een andere bijwerking van asparaginase is het optreden van allergische reacties. In de eerste kuur doet zich dit gewoonlijk niet voor omdat de patiënt hoge doses steroïden gebruikt. In de derde kuur kan zich dit echter wel voordoen.
Stamceltransplantatie
Bij de behandeling van ALL is er geen plaats meer voor autologe stamceltransplantatie. Bij alle patiënten met ALL wordt (afhankelijk van de co-morbiditeit) gestreefd naar een HLA-identieke allogene stamceltransplantatie van een familiedonor. Indien er geen familiedonor beschikbaar is zal er alleen gezocht worden naar een ongerelateerde donor voor een allogene MUD stamceltransplantatie bij een hoog risico of recidief. In de andere gevallen wordt voor onderhoudstherapie gekozen (HOVON 100). Bij patiënten ouder dan 40 jaar wordt uitsluitend gebruik gemaakt van een reduced intensity protocol.
Bij patiënten met een Philadelphia positieve ALL die een allogene stamceltransplantatie ondergaan, wordt de tyrosine kinase remmer in principe bij opname gestaakt en hervat na beenmergherstel en minimaal gedurende 6 maanden gecontinueerd. Hierna direct PCR, à 3 maanden, controleren.
Referenties
- Swerdlow et al. WHO classification of tumours of Haematopoietic and Lymphoid Tissues 2008.
- Pullarkat et al. Impact of cytogenetics on the outcome of adult acute lymphoblastic leukemia: results of Southwest Oncology Group 9400 Study. Blood 2008;111: 2563-72.
- Rowe JM. Optimal management of adults with ALL. British Journal of Haematology 2008;144: 468-83.
JHM_ALL_062 versie 4.
Geldig 3 juni 2014